
导语
在人工智能技术深度融入产业的当下,生物医药企业也都在将AI嵌入到传统的IT流程和系统中,以提升效率、赋能生产和服务。但当我们在享受AI带来的便利的同时,也需要关注其合规性和安全性,避免出现管理盲区、导致操作风险。因此,现阶段AI赋能(AI Enabled)的计算机化系统的合规管理成为了生物医药企业质量和IT部门的必修课。
凯莱英临床(凯诺)数字化创新团队和质量保证团队基于以往10多年的计算机化系统合规管理和服务经验,今天将从科学验证、数据治理、全生命周期管理等合规要点出发,结合ISPE GAMP® AI指南,分享对AI赋能计算机化系统的合规管理的实践思考,供行业同仁参考。
一、AI赋能计算机化系统的关键定义与框架
理解AI赋能计算机化系统的合规管理,首先需厘清核心术语与系统架构,这是开展合规工作的基础。
1.1核心术语
人工智能(AI):基于机器的系统,通过输入数据推断生成预测、决策等输出,部署后具备不同的自主性和适应性水平,是AI赋能系统的核心内核。
机器学习(ML):AI的核心分支,通过数据分析优化模型参数,无需明确编程即可实现模型迭代,是医药AI最常用的技术手段。
AI赋能(AI-Enabled)的计算机化系统:集成AI系统、非AI系统及其他组件的计算机化系统,是AI在医药领域落地的核心载体。
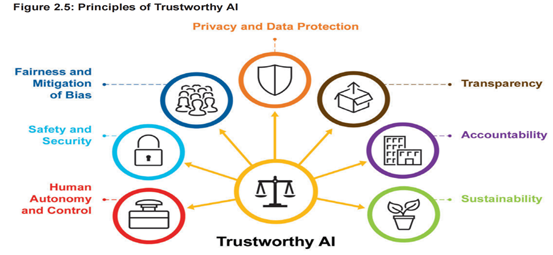
可信赖的人工智能:兼顾人类价值观的AI应用体系,是合规管理的重要导向。
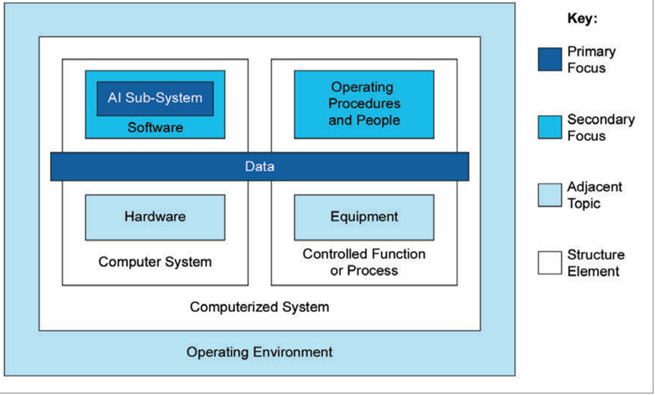
1.2 AI赋能的计算机化系统整体框架
系统由硬件、软件、数据、AI子系统、操作程序等多要素构成,AI子系统是核心、数据、硬件软件是支撑、人员与程序是关键,各要素相互关联,合规管理需覆盖全要素、全环节。
二、AI赋能的计算机化系统的生命周期管理
AI赋能计算机化系统的合规管理包括两个生命周期:
AI赋能计算机化系统生命周期:支持从概念化到退役的系统生命周期,涵盖概念阶段、项目阶段、运行阶段、退役阶段。这与传统计算机化系统生命周期一致。
AI子系统的模型开发生命周期:有别于传统计算机化系统生命周期,包含了数据管理,模型需求及设计、模型训练及模型测试。下图为AI子系统的模型开发生命周期。
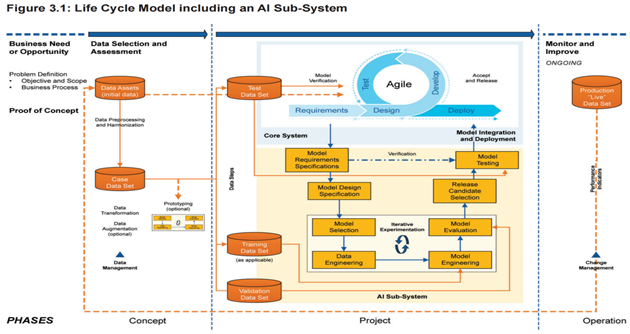
AI赋能计算机化系统包含(AI子系统)的项目阶段涵盖六大核心步骤,每个步骤均有明确合规要求,是系统从设计到落地的关键:
2.1、规划:
基于风险与复杂性确定开发规模,制定数据管理计划、模型迭代计划,建立验收标准(Acceptance Criteria)。
2.2、规范与设计:
模型需求规范以明确对模型性能的预期(KPI&Metrics),确保与GxP要求匹配、与整体系统无缝集成;对模型性能的预期(KPI&Metrics)如下指标(例如)。
准确度:是所有分类中正确的比例
召回率:所有实际阳性中被正确分类为阳性的比例
精确度:模型所有正分类中实际为正的比例
F1分数,即精确率和召回率的调和平均数
考虑包括为增量实验和迭代反馈过程定义一个终止标准
2.3、数据集创建及分割(Case Data Set Creation&Data Split):
划分训练集、验证集和测试集 (EMA GMP 附录22 对数据管理的要求)
训练数据集:数据用于从头训练模型或优化现有模型。
验证数据集:数据用于评估模型在模型工程步骤后性能,以指导后续开发过程或确定是否停止迭代实验过程
测试数据集:这些数据被提供给模型候选集, 以通过关键绩效指标(KPIs)对其性能特征进行最终评估
欧洲药品管理局在关于药品生命周期中的人工智能的反思文件中指出,测试集不能再次使用;而是应采用新的独立测试数据集
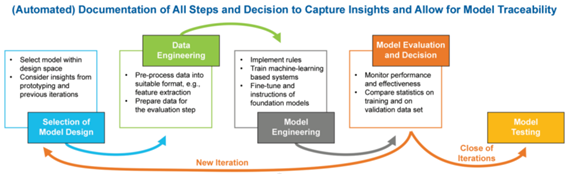
2.4、模型开发:
通过迭代实验完成模型选择、训练、微调,全程记录开发步骤,确保可追溯
2.5、验证:
验证活动除ISPE GAMP 5(第二版)中的附录D5[2]描述了计算机化系统测试之外,AI Enabled 的计算机化系统需要考虑以下额外方面:
将AI子系统所有者和其他技术专家(如人工智能和机器学习工程师)整合到测试活动
考虑针对人工智能特定功能和风险的额外特定测试类型
模型测试,以验证性能是否符合模型需求规范
验证活动包括将AI子系统(含模型)集成至AI Enabled计算机化系统,并对系统拟支持的业务流程层面进行需求测试
数据和模型可追溯性的验证、这包括模型输入、模型版本和模型输出之间的关系
2.6、报告和发布:
对于AI Enabled的计算机化系统而言,其核心在于整合迭代实验与模型测试结果,并涵盖用户验收测试中的人工智能特性。具体而言,这通常包括验证测试数据是否符合预期用途,以及描述模型测试过程中需求规格的满足程度。
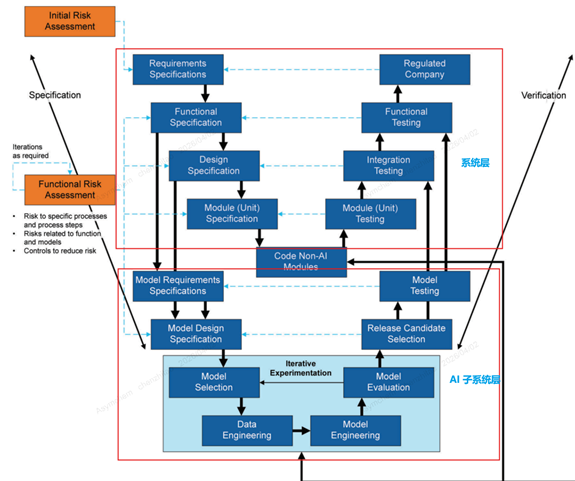
我们以定制化AI赋能的计算机化系统(GAMP Category 5)合规验证举例
定制化AI系统因复杂性高,是合规管理的重点,此类系统采用双层结构设计:
系统层:对整体需求、功能、设计进行规范验证,覆盖非AI组件与系统集成,符合GxP要求;
AI子系统层:针对模型设计、训练开展专项规范验证,确保模型性能满足业务需求。
两层结构通过功能、设计规范协同,最终通过集成测试和功能测试实现整体合规。
三、AI赋能计算机化系统合规管理的关键维度:AI成熟度
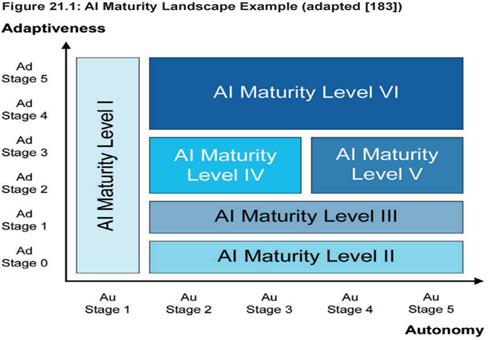
AI赋能计算机化系统的合规管理并非“一刀切”,需根据AI成熟度制定差异化合规策略,这是基于风险的质量风险管理核心要求,AI成熟度基于自主性与适应性的分级管理。
AI成熟度由自主性(自动执行任务能力)和适应性(自主迭代优化能力)两个维度构成,组合形成不同成熟度等级,不同等级对应不同控制策略:
• 低成熟度:人工全程干预,合规重点在操作规范与人工复核;
• 中成熟度:自动执行部分任务、需人工批准,合规重点在过程监控与数据追溯;
• 高成熟度:自动执行并自我优化,属于高风险AI系统,需建立严格的算法验证、性能监控、风险预警机制。
四、合规底线:AI赋能的计算机化系统风险防控与数据安全
AI为医药产业带来效率革命的同时,也带来了模型黑箱、数据泄露、算法偏见、网络攻击等新风险。企业必须坚持发展与安全并重,将风险防控和数据安全作为合规管理的底线,这也是国内外法规的共同核心要求。
4.1构建全生命周期质量风险管理体系
建立“风险识别-评估-控制-监控回顾”的闭环管理,针对AI子系统的功能风险、数据质量风险、模型漂移风险等制定针对性控制措施,同时将人类自主控制融入系统设计,保障操作人员的决策权。
4.2筑牢数据安全与隐私保护防线
数据是AI的核心,企业需建立完善的数据治理体系:确保训练/运行数据来源合法、质量可控;严格遵守数据隐私法规,对临床试验数据、生产核心数据等开展加密处理;建立分级保护机制;严禁涉密、敏感信息输入非涉密AI模型,防范泄露风险。
4.3强化网络安全与算法合规
AI系统面临对抗性攻击等新型网络威胁(如篡改影像数据、污染研发训练数据),企业需升级网络安全防护体系,运用AI提升主动防护能力;同时提升算法透明度和可解释性,完善算法备案制度,避免算法偏见带来的药品质量风险。
4.4建立完善的合规治理机制
明确AI子系统所有者、数据所有者、数据科学家、ML架构师等角色职责,提升全员AI素养与合规意识;完善模型/算法备案制度,开展定期合规审查和系统审计,确保系统持续合规运行。
结语
人工智能与医药产业的融合是大势所趋,各类法规则构建了AI赋能计算机化系统的合规框架。对于医药企业而言,唯有将合规管理融入AI系统的全生命周期,从核心定义、生命周期管理、成熟度分级、风险防控等多维度构建科学的合规体系,才能在享受AI技术红利的同时,守住药品质量和患者安全的底线。
以上是凯莱英(凯诺)数字化创新团队和质量保证团队的实践思考,欢迎各位行业同仁与我们交流,共同探讨AI赋能系统的合规之路。