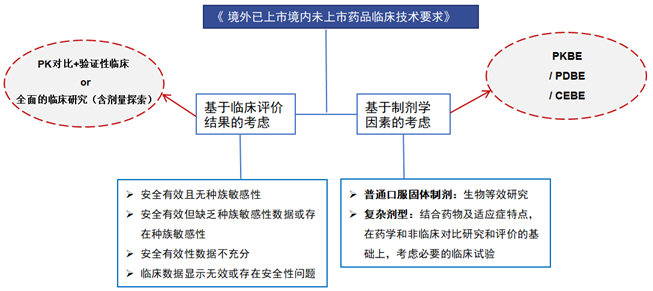
一、背景和现行要求 我国对于化学药品3类的临床要求经历过如下变革: 在2007年版注册管理办法实施期间,对于当时的化学药品3类和4类的临床评价要求为“应当进行人体药代动力学研究和至少100对随机对照临床试验。多个适应症的,每个主要适应症的病例数不少于60对”。 在2020年版注册管理办法实施之后,对于化学药品3类的临床评价要求不再以“药品注册管理办法配套附件”的形式发布,而是以“技术指导原则”的形式发布。根据《境外已上市境内未上市药品临床技术要求》,化学药品3类的临床评价要求分为两个部分,一是基于临床评价结果的考虑,另一个是基于制剂学因素的考虑。 基于临床评价结果的考虑,可能要求开展PK对比、验证性临床,或者包含剂量探索在内的全面的临床研究;基于制剂学因素的考虑,则可能要求开展生物等效研究,包括药代动力学终点的生物等效性研究(PKBE)、药效动力学终点的生物等效性研究(PDBE)、临床终点的生物等效性研究(CEBE)。图示如下: 下面,我们将从实操角度,逐一分析是否需要开展生物等效研究、PK对比研究及验证性临床研究。(注:仅存在种族差异时,才需要开展包含剂量探索在内的全面的临床研究,此种情形的临床路径比较明确,因此不做讨论)。 二、临床评价和实操考虑 • 2.1 是否需要开展生物等效性研究的考虑 1) 对于口服固体制剂,应根据指导原则的要(CDE&ICHM13),开展生物等效性研究; 2) 根据《ICH M9:基于生物药剂学分类系统的生物等效性豁免》,对于全身作用的口服固体制剂,剂型和规格与参比制剂相同的情况下,可适用于基于 BCS 分类的生物等效性豁免; 3) 对于复杂制剂,需要根据品种和适应症特点,在药学和非临床对比研究和评价的基础上,考虑必要的临床试验; 4) 参考 FDA 个例指南的要求。 • 2.2 是否需要开展 PK 对比研究的考虑 1) 原则上,在验证性临床之前需要首先获得中国人群的 PK 特征数据; 2)如果在PKBE 研究中已获得中国人群PK 特征,呈现线性 PK关系时,应与 原研进行PK对比:如果PK特征差异小,豁免PK对比;如果PK特征差异大,单/多次PK对比;如果有一定的差异、但有把握的情况下,可在验证性临床中开展popPK建模; 3)原研审评报告及上市后发表的高质量文献报道中,有充分的中国人群PK特征数据、证明PK特征无种族差异,可以豁免PK对比研究; 4)对于不适合开展PK研究的剂型(如局部作用局部起效药物),可以豁免 PK对比研究; 5)基于公平性原则考虑。 • 2.3 是否需要开展验证性临床研究的考虑 1) 考虑目标化合物是否在国内上市:对于真3类化学药品,通常需要开展验证性临床研究; 2) 全球数据中已有中国人群PK、和/或PD、有效性和安全性数据,且经分析认为其用于中国患者的获益大于风险的,可以豁免验证性临床; 3) 拟用于严重或危及生命疾病、罕见病且无有效治疗手段的药品,或用于此类疾病且较现有治疗手段具有明显提高疗效或安全性等优势的药品,且不存在种族差异,可申请附条件批准; 4) 在适应症相同的前提下,国内已有其他剂型/给药途径/用法用量获批上市,通过剂量-暴露-效应关系的桥接,可以充分评价新剂型/给药途径/用法用量的安全性和有效性,可以减或免临床试验。 5) 基于公平性原则考虑。 三、思考和未来展望 目前,由于我国数据保护政策尚未落地(如下图),因此仍需基于公平性原则重复开展验证性临床,才能支持上市申请。 如果数据保护政策落地之后,笔者猜测: 1)对于一个全新的化药3类品种,首家完成验证性临床上市后,会获得3年的数据保护。如后续企业仍坚持提出上市申请的,也可以重复开展验证性临床,并获得一定期限的“搭便车”保护;否则,可在首家保护期届满前一年内提出依赖其验证性临床数据的上市申请,无需重复开展验证性临床。 2)对于既往已开展过验证性临床的品种,笔者认为“追加”数据保护的可能性不大。数据保护制定的初衷是为了避免重复开展临床试验造成资源浪费,因此对于这类品种,可能会豁免验证性临床。 药政法规事务部 CLIN-NOV 全球药政法规事务部团队成员来自MNC药厂,平均拥有10年以上的工作经验,能深刻理解中美欧澳等法规要求,在INTERACT Meeting,ODD,IND,EOP1,EOP2,NDA等申请流程、文件质量把控,及与监管沟通技巧上有丰富的经验。部门承接了多项中美双报项目,包括双抗、单抗、重组蛋白、ADC、PDC、小分子,小核酸等,适应症涵盖实体瘤、血液瘤,干眼症、感染类疾病、代谢类疾病、自身免疫性疾病等。团队成员在CMC,非临床及临床层面拥有强大的技术综合背景,能够根据不同产品的作用机制及开发阶段,从全局观出发提供合理的产品的开发路径及与监管沟通的策略。另外,团队有丰富的专家资源,包括前CDE的评审专家及前FDA审评员等,能够从技术及法规的双重层面,持续为项目保驾护航。